頭脳循環プログラム

プログラムの概要
頭脳循環を加速する戦略的国際研究ネットワーク推進プログラム
プログラム名:酸化ストレス仮説に基づく新規精神疾患創薬のための国際共同研究(S2603)
が2014年10月1日付けで、採択(内定)されました。
本プログラムは、国際共同研究ネットワークの核となる優れた研究者を育成し、我が国の学術の振興を図ることを目的とし、大学等研究機関が、海外のトップクラスの研究機関と世界水準の国際共同研究を行うことを通じて、相手側への若手研究者の長期派遣と相手側からの研究者招へいの双方向の人的交流を展開する取組を支援するもので、概要はつぎのとおりです(下記サイトの内容を簡潔にまとめます)。
http://www.jsps.go.jp/j-zunoujunkan3/data/saitakujigyou/h26/S2603_gaiyo_osaka.pdf
1. 事業の背景
統合失調症やうつ病などの精神疾患は、自殺や就学・就労困難などの社会的損失をもたらす重要疾患ですが、依然、薬剤の治療貢献度・治療満足度の低い疾患で、原因解明と新しい概念に基づく創薬が焦眉の課題です。一方、阪大では、PACAPという脳に強発現する神経ペプチドの研究で、その変調を統合失調症の脆弱性に関わる情動・認知機能障害のリスク因子として同定するほか、その下流分子(新規のミトコンドリア動態制御因子を含む)から成るPACAPシグナルが、酸化ストレス仮説を含む精神疾患の病因仮説に関わることを示し、都医学研では、糖やアミノ酸の酸化等による蛋白質修飾反応(カルボニルストレス)が約2割の統合失調症患者に認められ、それにビタミン B6の減少等が関連することを明らかにすることで、同病の生物学的な理解と新規治療法の提案を推進してきました。
2. 事業の目標
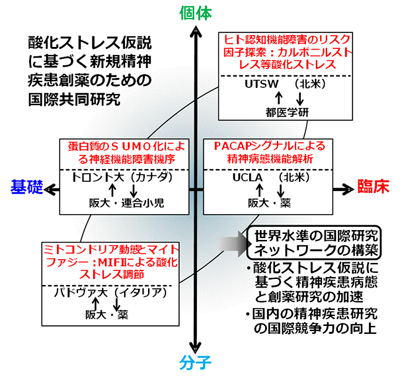
これら阪大、都医学研の研究グループによる、統合失調症やストレス障害における神経ペプチド PACAPシグナル、カルボニルストレス(酸化ストレスの一種)の発見を基盤とし、これに関連するミトコンドリアの動態・機能調節、蛋白翻訳後修飾等をあわせた病態機序を究明し、精神障害発現機序を多角的に解明する国際共同研究の枠組みを構築することを目標とします(下図参照)。そして、日本での当該研究を推進し、精神疾患の成因となる酸化ストレス等による神経機能・発達障害の疾患概念確立ならびに創薬研究の展開を目指します。
3. 事業の特色
本プログラムには、ミトコンドリア動態研究あるいはヒト高次認知機能研究をリードするイタリア・パドヴァ大、北米UTSWの研究グループと、精神・神経疾患のモデル動物研究で独創性が高い研究を行う北米UCLAの研究者、アルツハイマー病における神経障害研究の第一人者(カナダ・トロント大)が参画します。本計画で達成される、研究室の中堅研究者の長期派遣を中心とした相互連携体制の実現により、世界水準の高密度な研究展開と国際競争力の大幅な向上が実現すると考えられます。
4. 事業の推進方法
海外の4つの連携機関に准教授等を長期派遣し、神経の機能調節・障害についてマイトファジー(酸化ストレス源となる機能低下したミトコンドリアの廃棄機構)の調節等から多角的に究明するほか、分子レベルの基礎的知見を個体レベルや臨床研究に有機的に結び付けるため、蛋白質の翻訳後修飾やPACAP3 型受容体(発現増加が一部の統合失調症の発症要因(Nature 2011))の研究、ヒト認知機能障害に関わるリスク因子の同定や解析研究を行います。また海外からの研究者招へいを通じて日本国内の関連研究を加速させるとともに、4 か国の各機関相互の情報を共有し、本疾患領域での頭脳循環を実現します。
以上、研究期間は2016年度まで、このような新規精神疾患創薬のための国際共同研究を行い、その成果を論文や学会等で発表します。またその途中でも、種々のセミナーやシンポジウムを利用して、研究の結果を分かりやすく説明して行きたいと考えています。